Ao longo deste artigo, exploraremos os aspectos essenciais para a correta avaliação do desempenho dos indicadores biológicos com tempo de resposta reduzido, focando na metodologia de detecção por fluorescência e nos desafios envolvidos na sua validação.
É fundamental compreender como os esporos viáveis são identificados nas diferentes tecnologias atualmente utilizadas em indicadores biológicos para a avaliação da eficácia do processo de esterilização.
Um dos métodos de detecção baseia-se na mudança de cor do meio nutritivo, um fenômeno resultante da redução do pH provocada pelo metabolismo dos esporos viáveis em crescimento. Em meios específicos, essa atividade metabólica altera a coloração do líquido de roxo para amarelo, indicando a presença de microrganismos viáveis.
Outra abordagem para antecipar a detecção de esporos é a utilização de reações enzimáticas que geram fluorescência. Nesse caso, as enzimas presentes ou liberadas pelos esporos viáveis desencadeiam a síntese de substâncias fluorescentes, que podem ser detectadas já nas primeiras horas de incubação por meio de equipamentos compatíveis, como o Auto-Reader Clean Test®.
A obtenção de resultados antecipados, no entanto, exige rigorosa qualidade dos indicadores biológicos, pois a confiabilidade dessa antecipação é essencial para garantir a segurança do processo e evitar interpretações errôneas que possam comprometer a avaliação da esterilização.
Entendendo os conceitos para avaliação de Indicadores Biológicos com Tempo de Incubação Reduzido:
Os padrões de saúde definiram o tempo de incubação tradicional para IB’s em 7 dias. Períodos de incubação mais curtos são permitidos, desde que o Tempo de Incubação Reduzido (RIT, em inglês) tenha sido validado.
O tempo final de incubação é o período mínimo de cultivo necessário antes de fazer uma determinação de que um indicador biológico é negativo (não mostra crescimento). A norma ISO11138-1 afirma que o tempo de incubação deve ser validado pelo fabricante do indicador biológico.
Um método para validar o RIT foi publicado no Anexo II da orientação “Biological Indicator (BI) Premarket Notification [510(k)] Submissions, 04 de outubro de 2007. Guide for Validation of Biological Indicator Incubation Time” da FDA, também está descrito na norma ISO 11138-8: 2021. Este protocolo é apropriado para todos os tipos de IB’s com um tempo de leitura inferior a 7 dias.
A orientação exige que os fabricantes exponham um total de 300 unidades de IB’s (100 IB’s de 3 lotes diferentes) a condições parciais no ciclo de esterilização apropriado, a fim de produzir uma mistura de resultados positivos e negativos. Um ciclo parcial é descrito como um ciclo no qual todos os parâmetros de esterilização, exceto o tempo, são atendidos e visa simular um processo falho de esterilização. Dessa forma, o fabricante deve identificar um ciclo de esterilização parcial no qual 30% a 90% dos Indicadores Biológicos sobrevivem. Neste cenário, a norma enfatiza que a precisão do resultado deve ser acima de 97%.
Deve-se considerar que os esporos que sofrem processos de esterilização podem estar danificados, mas não mortos. Seu reparo requer um período mais longo e sua germinação é tardia em relação a esporos intactos. Isso prolonga o tempo de incubação e, portanto, uma avaliação confiável. Por isso, o teste de eficácia do produto deve ser realizado nesse parâmetro, sendo neste estado em que os resultados da redução do tempo de incubação têm sua veracidade afirmada.
Quando o indicador biológico não possui qualidade adequada, pode ocorrer um falso negativo, ou seja, esporos viáveis não são detectados, levando à falsa impressão de que o processo de esterilização foi eficaz. Isso pode acontecer porque, em algumas condições de esterilização parcial, os esporos podem não produzir ou liberar enzimas em quantidade suficiente para desencadear a reação fluorescente dentro do período reduzido de incubação. Dessa forma, mesmo que ainda haja esporos viáveis, a ausência de fluorescência pode levar à conclusão errônea de que não houve crescimento microbiano. No entanto, com a incubação prolongada, esses esporos podem se manifestar posteriormente pela mudança de cor do meio nutritivo, evidenciando que a antecipação do resultado foi incorreta e que o produto deveria ter sido retido para avaliação adicional.
Já procurou saber se o fabricante da sua marca de Indicador Biológico segue a risca as normativas de validação?
A norma vigente direciona que a validação dos IBs deve se concentrar nos indicadores submetidos a esterilizações parciais, pois são esses que realmente determinam a eficácia do tempo reduzido de incubação. Indicadores biológicos do tipo controle (que não passam pelo processo de esterilização) e aqueles totalmente esterilizados são facilmente identificáveis – os primeiros sempre darão positivo, e os segundos sempre negativo. No entanto, a grande complexidade está na detecção dos esporos que passaram por um processo de esterilização falho ou parcial. Esses sim devem ser testados e validados com rigor, pois representam as situações críticas onde a detecção precoce faz toda a diferença na segurança do processo.
Dessa forma, embora a antecipação dos resultados traga benefícios operacionais e econômicos, ela deve ser realizada com extremo cuidado e validação adequada. A confiabilidade do tempo reduzido de incubação depende de rigorosos protocolos científicos para garantir que esporos danificados ainda possam ser detectados e que o sistema não apresente falsos positivos ou negativos. Apenas um controle rigoroso desses fatores assegura que a redução do tempo de incubação não comprometa a segurança e eficácia dos processos de esterilização.
Então, como evidenciar a eficiência do processo para o seu IB de resposta rápida por fluorescência ?
O resultado do Indicador Biológico (IB) de resposta rápida quanto à eficiência do processo de esterilização se dá através de dois mecanismos químicos por meio da interação com os esporos viáveis em crescimento: O primeiro é uma reação enzimática oriunda de esporos viáveis que desencadeia a síntese de substância fluorescente que pode ser identificada nos minutos iniciais da incubação através de uma incubadora compatível, no caso desse teste a Auto-Reader Clean Test®. O segundo mecanismo é um processo de mudança de cor do caldo nutritivo de roxo para amarelo durante a incubação induzido pela redução do PH do meio através da interação com os esporos viáveis, esse processo serve como confirmação de resultado e pode ocorrer em até 48 horas após a incubação.
Testes de conformidade podem ser realizados com base na norma ISO 11138-8:2021, garantindo que a antecipação dos resultados seja avaliada de forma precisa e confiável. O objetivo desses testes é verificar o desempenho dos indicadores biológicos em situações críticas de esterilização, onde a eliminação total dos esporos não ocorre. Nessas condições, os poucos esporos remanescentes no sistema do indicador biológico devem ser capazes de gerar um resultado positivo, e a incubadora de reposta rápida deve ser capaz de detectar este sinal, evidenciando falhas no processo de esterilização sempre que necessário.
Recomendamos que a realização dos testes seja acompanhada por um profissional especializado. É essencial compreender que, durante esses testes, os materiais utilizados não devem ser destinados ao uso posterior, uma vez que o objetivo não é a esterilização efetiva, mas sim a avaliação da qualidade e desempenho dos indicadores biológicos.
A Clean-Up demonstra abaixo os resultados obtidos para os testes dos seus indicadores biológicos de resposta rápida.
O Gráfico 1 apresenta a resposta fluorimétrica de um Indicador Biológico de Resposta Rápida Clean Test Vapor 1 hora – Controle, que não foi exposto ao processo de esterilização.
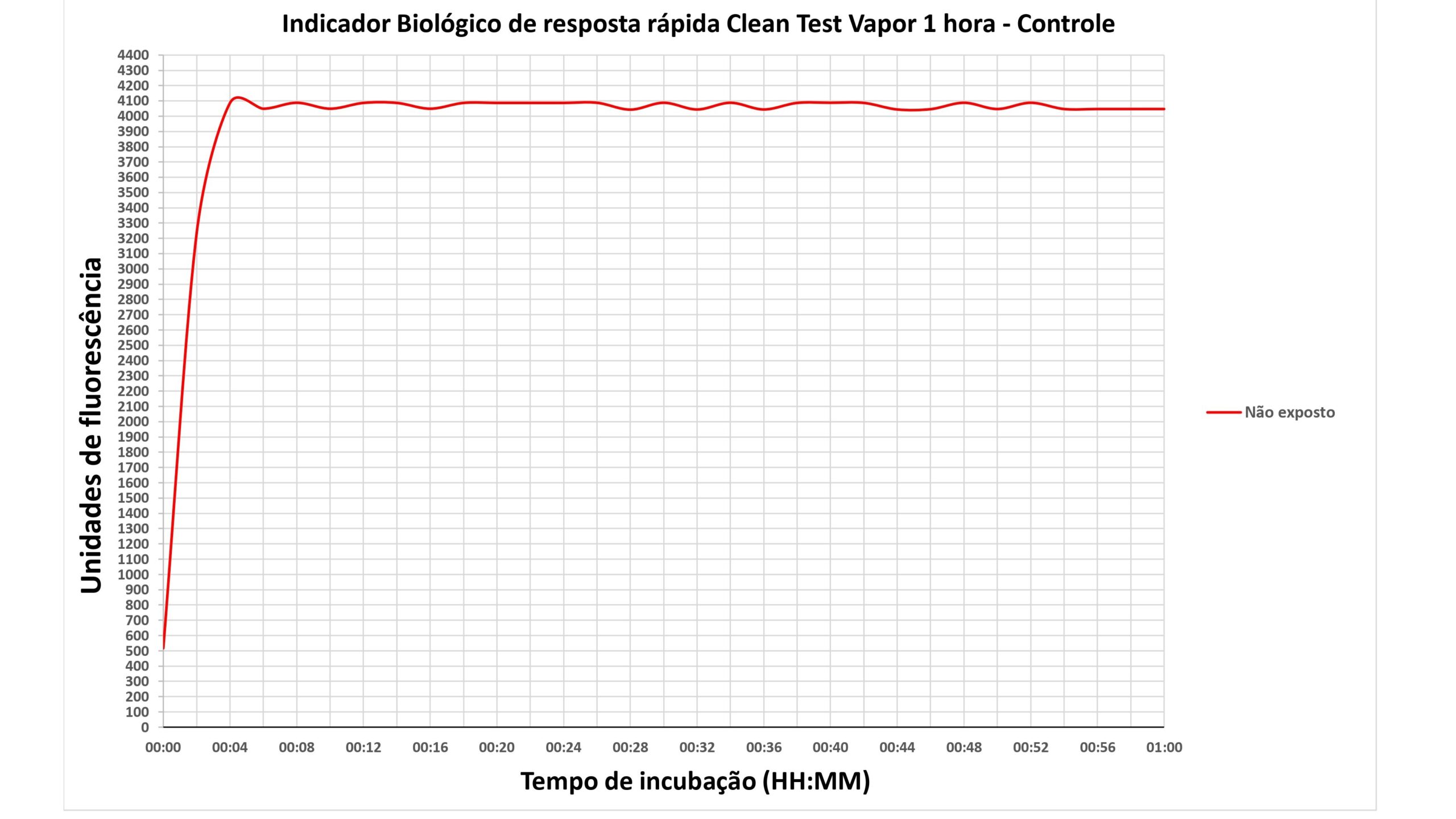
O gráfico acima demonstra a relação direta entre o tempo de incubação e as unidades de fluorescência, evidenciando que, já nos primeiros 4 minutos de incubação, ocorre um crescimento em torno de 4000 unidades de fluorescência, caracterizando o indicador biológico como positivo, com uma população bacteriana sobrevivente estimada em aproximadamente 10⁶ (1 milhão) UFC (Unidade Formadora de Colônia).
A presença de unidades de fluorescência está diretamente relacionada à produção de um composto fluorescente resultante da reação enzimática mediada pela α-glucosidase presente na parede dos esporos viáveis. Essa reação permite a antecipação da resposta rápida do indicador biológico, uma vez que a enzima α-glucosidase, ligada à parede do esporo, possui resistência equivalente à do próprio esporo. Isso estabelece uma correlação direta entre a atividade enzimática e o potencial crescimento microbiano futuro.
O Gráfico 2 representa a resposta fluorimétrica de um Indicador Biológico de Resposta Rápida Clean Test Vapor 1 hora, que foi submetido a uma exposição letal em BIER Vessel, tornando-se estéril.
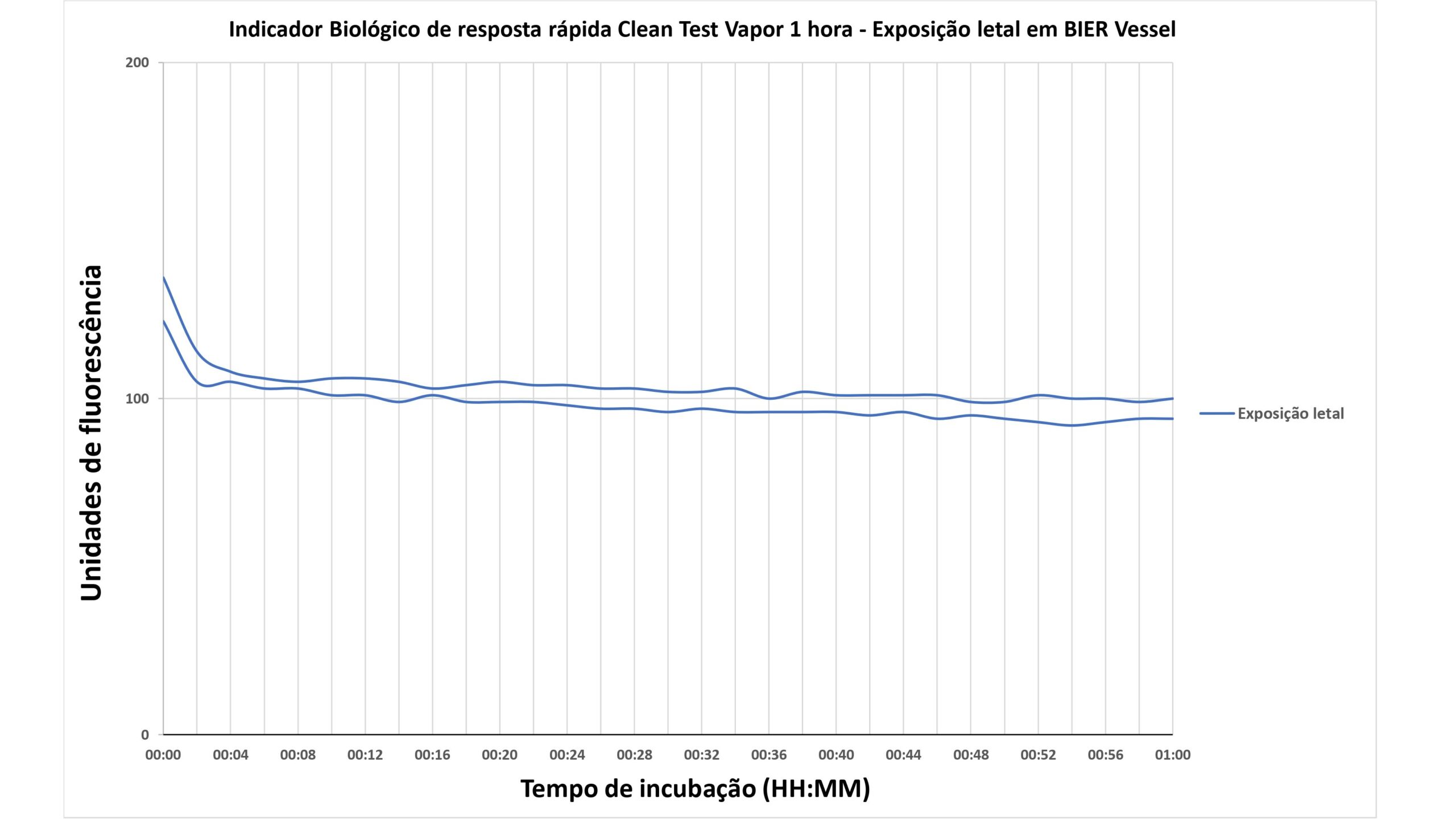
Nesse cenário, observa-se a ausência de crescimento de unidades de fluorescência ao longo de 1 hora de incubação, com os valores de leitura permanecendo próximos a 100 unidades de fluorescência, a qual referencia-se ao ponto inicial de partida (referência inicial).
Dessa forma, é possível correlacionar a resposta de fluorescência com um indicador biológico estéril, ou seja, com um resultado negativo, confirmando a eficácia do processo de esterilização.
O Gráfico 3 apresenta várias curvas de resposta de fluorescência de um Indicador Biológico de Resposta Rápida Clean Test Vapor 1 hora ao longo do período de incubação de 1 hora.
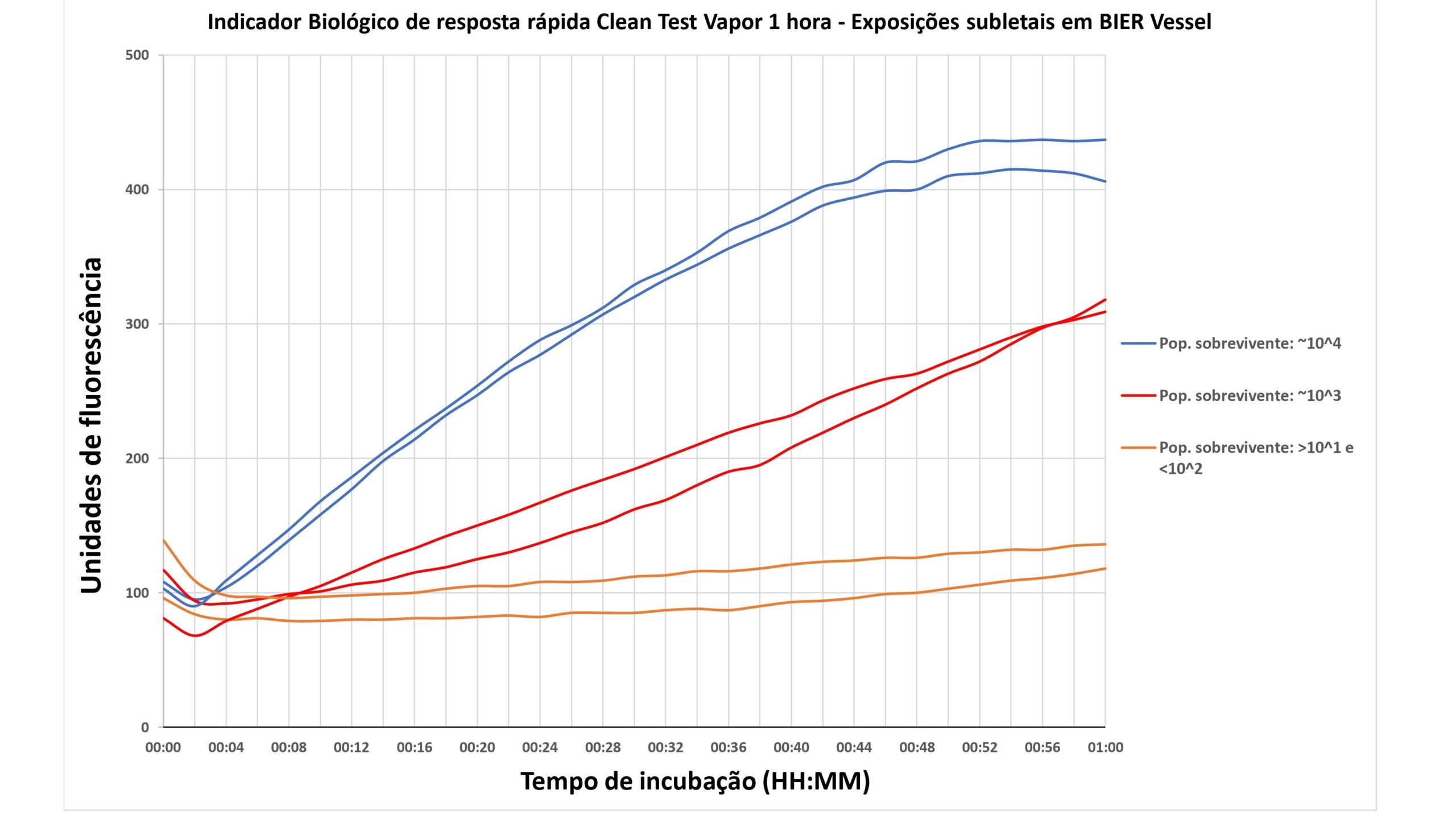
Os três padrões de curvas são divididos da seguinte forma:
– Pop. sobrevivente: ~104
Neste padrão, duas unidades de Indicador Biológico de resposta rápida Clean Test Vapor 1 hora foram submetidos a uma exposição subletal intensional em BIER Vessel, de tal forma que a população biológica sobrevivente em cada IB foi de aproximadamente 104 (10 mil) UFC, ou seja, houve uma redução de 2 Log’s da população inicial, simulando um processamento falho.
Durante a incubação destes IB’s (curvas em azul no Gráfico 3) é possível observar um expressivo crescimento de fluorescência ao longo do período de incubação de 1 hora, saltando de cerca de 100 unidades em 2 minutos para mais de 400 unidades de fluorescência ao final do período de incubação. Esse crescimento das unidades de fluorescência está diretamente relacionado à população biológica sobrevivente no indicador biológico, indicando que o IB é positivo e houve uma falha no processo de esterilização.
– Pop. sobrevivente: ~103 e Pop. sobrevivente: >101 e <102
Nestes demais casos, foi repetido o processo em BIER Vessel descrito anteriormente com unidades de Indicador Biológico de resposta rápida Clean Test Vapor 1 hora de tal forma que foi obtido duas unidades de IB com população biológica sobrevivente de aproximadamente 103 (1 mil) UFC (curva em vermelho no Gráfico 3) e duas unidades com população biológica sobrevivente entre 101 e 102 (10 e 100, respectivamente) UFC (curva em laranja no Gráfico 3).
Em ambos os casos é possível observar crescimento de unidades de fluorescência (mesmo que pequeno nos casos dos IBs com pop. sobrevivente: >101 e <102) e, consequentemente, crescimento biológico, indicando que os indicadores biológicos em questão são positivos.
A análise gráfica evidencia de forma clara que a reação enzimática mediada pela α-glucosidase, presente na parede dos esporos viáveis, é um mecanismo altamente eficaz para a antecipação da resposta de crescimento microbiano em Indicadores Biológicos de Resposta Rápida Clean Test. Além disso, reforça a importância de validar essa metodologia para quaisquer outros indicadores biológicos de resposta rápida disponíveis no mercado. Para garantir a confiabilidade desses sistemas, a eficiência da antecipação da fluorescência deve ser rigorosamente testada em cenários de exposição subletal, onde a detecção da atividade enzimática é mais desafiadora. Apenas dessa forma é possível assegurar que os indicadores biológicos de resposta rápida sejam precisos, confiáveis e adequados para a avaliação da eficácia dos processos de esterilização.

